| |

Dosage de l'éthanol
dans l'aquarium.
Voies nouvelles pour l'amélioration des
conditions de vie.
par Michael Mrutzek et Jörg Kokott ©
 Depuis des décennies nous essayons d'améliorer les
conditions de maintenance de nos coraux et de nos poissons. De
nouveaux articles parlent de progrès, de nouvelles techniques et de
moyens qui doivent nous permettre d'améliorer la qualité de vie de
nos pensionnaires. Depuis plus de deux ans l'un des auteurs (Michael
Mrutzek) travaille sur une méthode, afin d'améliorer la dégradation
des importantes quantités de nitrates dans les aquariums d'eau de
mer et par là même les conditions de vie des animaux d'aquarium. Les
enseignements récoltés sont relatés et étayés par des connaissances
théoriques. Depuis des décennies nous essayons d'améliorer les
conditions de maintenance de nos coraux et de nos poissons. De
nouveaux articles parlent de progrès, de nouvelles techniques et de
moyens qui doivent nous permettre d'améliorer la qualité de vie de
nos pensionnaires. Depuis plus de deux ans l'un des auteurs (Michael
Mrutzek) travaille sur une méthode, afin d'améliorer la dégradation
des importantes quantités de nitrates dans les aquariums d'eau de
mer et par là même les conditions de vie des animaux d'aquarium. Les
enseignements récoltés sont relatés et étayés par des connaissances
théoriques.
La donnée du problème est simple : comment
puis-je diminuer la charge en nitrates de l'aquarium sans renoncer à
la population piscicole et sans être obligé de recourir à une
importante technique.
Les méthodes du passé
Au
cours des 18 dernières années les filtres à nitrates ont entrepris
d'éliminer avec efficacité les nitrates accumulés dans l'eau. Cette
composante technique supplémentaire est dépendante du type et du bon
fonctionnement du produit et en outre liée à un important mécanisme
de contrôle.
Avec l'aquarium Miniriff de De Hahn (Miniriff,
Hollande) les filtres à nitrates ont fait leur entrée dans les
aquariums. A l'époque Miniriff Hollande a construit le premier
filtre à nitrates alimenté par une solution alcoolique placée dans
un sachet nutritif. Le sachet lui-même est constitué par une
membrane semi-perméable, qui diffuse la solution alcoolique et
approvisionne en permanence les bactéries durant plus de quatre
semaines. Le filtre à nitrates est constitué par un système à
plusieurs compartiments, l'eau traversant chaque compartiment
individuel, le dernier compartiment ne comportant plus de sachet,
afin que les substances nutritives restantes puissent être
décomposées, si bien que celles-ci ne parviennent pas dans
l'aquarium.
Quelques années plus tard un autre filtre à
nitrates fonctionnant sur la base des "Baktoballs" (AquaMedic) a
fait son apparition sur le marché. Il s'agit d'un système avec un
compartiment unique, dans lequel on introduit des Bioballes et une
quantité définie de "Baktoballs".
D'autres sociétés ont
construit des systèmes plus ou moins similaires. Il y a cinq ans le
Vodkafilter de Lars Sebralla a fait son apparition, lequel a été
présenté la première fois lors du Symposium de Lünen.
Celui-ci
fonctionne également sur la base d'une solution alcoolique, mais qui
n'est pas fournie par un ensemble de substances nutritives, mais par
l'intermédiaire d'une pompe. La différence notable se situe dans le
système de circulation, une partie seulement de l'eau provenant du
filtre étant ramenée à la circulation de l'eau.
 Il ne faut pas oublier le filtre à nitrates basé sur
le soufre qui a vu le jour ces dernières années. Tous les systèmes
décrits jusqu'à présent hébergent des dénitrificateurs
hétérotrophes, ce qui signifie, que contrairement aux plantes ils ne
peuvent pas créer eux-mêmes leur nourriture par utilisation de
l'énergie solaire, mais qu'ils doivent manger de façon active. Dans
le filtre sur soufre les dénitrificateurs autotrophes croissent par
contre, n'utilisant certes pas la lumière solaire, mais l'énergie
provenant de l'oxydation du soufre élémentaire. Les bactéries n'ont
pas besoin d'être nourries. Lors de l'oxydation du soufre
élémentaire les bactéries produisent de l'acide sulfurique (H2SO4),
qui est neutralisé dans une colonne de calcaire installée en sortie.
D'une part le filtre sur soufre permet une dégradation des nitrates,
d'autre part il fonctionne comme un réacteur à calcaire, ce qui peut
mener à des problèmes de quantité de calcium et de dureté
carbonatée. Il ne faut pas oublier le filtre à nitrates basé sur
le soufre qui a vu le jour ces dernières années. Tous les systèmes
décrits jusqu'à présent hébergent des dénitrificateurs
hétérotrophes, ce qui signifie, que contrairement aux plantes ils ne
peuvent pas créer eux-mêmes leur nourriture par utilisation de
l'énergie solaire, mais qu'ils doivent manger de façon active. Dans
le filtre sur soufre les dénitrificateurs autotrophes croissent par
contre, n'utilisant certes pas la lumière solaire, mais l'énergie
provenant de l'oxydation du soufre élémentaire. Les bactéries n'ont
pas besoin d'être nourries. Lors de l'oxydation du soufre
élémentaire les bactéries produisent de l'acide sulfurique (H2SO4),
qui est neutralisé dans une colonne de calcaire installée en sortie.
D'une part le filtre sur soufre permet une dégradation des nitrates,
d'autre part il fonctionne comme un réacteur à calcaire, ce qui peut
mener à des problèmes de quantité de calcium et de dureté
carbonatée.
Systèmes alternatifs
Tous les
filtres à nitrates brièvement décrits nécessitent pour leur
fonctionnement un déploiement technique considérable, un contrôle
particulier de la vitesse de circulation de l'eau, de la quantité de
nourriture ainsi qu'une surveillance du potentiel Redox.
En
ce qui concerne la thématique des filtres à nitrites il faut
mentionner les filtres sur lit de sable. Les Deep Sand Beds (DSB)
très utilisés aux USA, le classique système Jaubert tout comme le
récent système de filtration sur vase (Désignation commerciale :
Miracle Mud) fonctionnent comme des filtres à nitrates. Le substrat
devient anoxique (sans oxygène) au sein de quelques centimètres dans
des couches de sédiments suffisamment épaisses en dépendance avec la
vitesse du courant au-dessus des sédiments. Ici vivent les bactéries
hétérotrophes qui dénitrifient les nitrates en azote moléculaire
(N2). Finalement, il s'y produit la même chose que dans un filtre à
nitrates, toutefois dans un environnement naturel et sans autre
moyen technique et avec un entretien faible, ce qui a rendu ces
systèmes de filtration très populaires. Dans ce cas les bactéries
sont également dépendantes d'une source de carbone, à laquelle elles
peuvent accéder à un dépôt riche en carbone dans les sédiments en
règle générale avec les dépôts de carbone organique particulaire
(POC, anglais : Particulate Organic Carbon) sous la forme de
détritus, de restes d'algues et de mini-faune décédée.
Sans filtre extérieur
Les réflexions ont été
poussées dans une autre direction, car nous souhaitions une variante
plus simple, sans filtre extérieur, donc une utilisation directe
dans l'aquarium. Dans chaque système "rodé" vivent des bactéries,
qui s'occupent aussi bien de la nitrification que de la
dénitrification. Elles vivent dans des films biologiques (biofilms),
qui recouvrent toutes les surfaces de l'aquarium y compris les
vitres et l'intérieur des tuyauteries. Cependant en règle générale,
seul le sol et les pierres décoratives permettent la présence des
nitrificateurs et des dénitrificateurs, car là seulement la surface
du matériel est si importante qu'à côté des zones aérobies, des
zones anaérobies peuvent également se développer. Au cours de la
dernière décennie il s'est de plus en plus vérifié que les pierres
récifales vivantes constituaient le matériel de décoration le plus
approprié, surtout en raison de sa multiplicité en souches
bactériennes et en microorganismes.
Ceci constitue
exactement le point de départ, car à l'intérieur des "pierres
vivantes" une décomposition des nitrates est directement possible
dans le système. Il s'agit seulement de favoriser celle-ci.
 |
|
Ethanol
(CH3CH2OH) |
Les premières
expériences
Les expériences ont démarré avec du miel, car à
l'époque Michael Mrutzek pensait que les acides aminés contenus dans
le miel d'apiculteur approvisionnerait le système non seulement en
carbone mais en même temps en une forme d'azote organique. Toutefois
le dosage exact constituait un problème permanent et le succès
escompté relatif aux acides aminés n'a pas été convaincant, raison
pour laquelle les essais avec le miel ont été stoppés. A la
recherche d'autres sources carbone la vodka est entrée dans jeu. Au
départ Michael Mrutzek a injecté 1 ml de vodka dans son aquarium
privé de 1000 litres, car il n'était pas évident de prévoir la
réaction de l'aquarium. Cette quantité a été ajoutée tous les matins
durant une semaine.
Après la phase d'observation, le dosage a
été augmenté tous les 3 jours d'abord à 2 puis 3 ml, 4 ml jusqu'à 15
ml étalé sur une totalité de 40 jours. Même avec 15 ml aucune
modification négative n'a été visible, toutefois des développements
plutôt positifs car les coraux présentaient un meilleur aspect. Les
coraux mous, les gorgones, les anémones disques et les
scléractiniaires montraient des polypes nettement plus épanouis.
Durant l'intégralité de la période d'essais les paramètres de l'eau
ont été contrôlés tous les 3 jours. A ce moment, la quantité de
nitrates de 12,5 mg/l départ a chuté à 2,5 mg/l et la quantité de
phosphates de 0,1 mg/l à 0,05mg/l.
 Après qu'avec 15 ml/jour aucun effet secondaire négatif
n'a été constaté, l'augmentation à 16 ml a été effectuée ce qui a eu
comme suite que le jour suivant une légère turbidité de l'eau a été
constatée et qu'un dépôt mucosique recouvrait les vitres et la
décoration. Dès ce moment l'écumeur a été immédiatement accéléré et
l'additif de vodka arrêtée. Le lendemain la turbidité était encore
reconnaissable et le dépôts mucosique encore présent, mais plus
aussi important que la veille. 24 heures plus tard tout avait
disparu. Après qu'avec 15 ml/jour aucun effet secondaire négatif
n'a été constaté, l'augmentation à 16 ml a été effectuée ce qui a eu
comme suite que le jour suivant une légère turbidité de l'eau a été
constatée et qu'un dépôt mucosique recouvrait les vitres et la
décoration. Dès ce moment l'écumeur a été immédiatement accéléré et
l'additif de vodka arrêtée. Le lendemain la turbidité était encore
reconnaissable et le dépôts mucosique encore présent, mais plus
aussi important que la veille. 24 heures plus tard tout avait
disparu.
Un troisième jour de répit a été respecté afin ensuite
de commencer de nouveau le dosage, toutefois uniquement avec 14 ml.
Un jour plus tard la turbidité était revenue. Un examen des
paramètres de l'eau n'a pas permis de mettre en évidence des
nitrates ou des phosphates mesurables.
La quantité de
calcium et de magnésium
La valeur du pH ainsi que la dureté
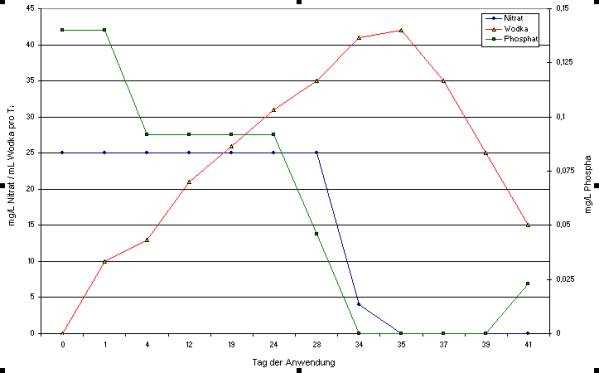
carbonatée se situaient dans la zone normale. Le diagramme
montre la modification de la quantité de substances nutritives en
dépendance avec le dosage en éthanol. En même temps devient visible
le rapport inversement proportionnel entre la quantité de nitrates
et le dosage en éthanol (coefficient de relation – 0,95). Après un
certain ralentissement la quantité de nitrates devient linéaire par
rapport à l'augmentation de la concentration d'éthanol. Cette
constatation montre l'effet direct du dosage du carbone sur les
dénitrificateurs. Par contre la quantité de phosphates chute
graduellement avec l'augmentation linéaire de la concentration
d'éthanol (coefficient de corrélation – 0,87), ce qui laisse
supposer que la croissance des bactéries se produit dans ce cas en
poussées définies. Si on observe la formation et le développement
d'un film biologique, le substrat d'établissement se transforme
rapidement en facteur limitant dans le cas d'une multiplication
rapide de la population et la croissance ralentit. Lorsque des
parties du film biologique sont arrachées ou que les bactéries
meurent, il y de nouveau de la place et la multiplication des
bactéries peut faire un bond, ce que reflète peut-être le
déroulement de la courbe des phosphates.
Il est facile de
comprendre que les bactéries ont utilisé l'ensemble des substances
nutritives pour leur croissance et leur importante multiplication.
Contrairement à la croyance largement répandue, que l'eau des
aquariums contient assez de composés carbonés organiques, notre avis
est différent.
Après qu'au bout de deux jours, l'eau était de
nouveau limpide, que les poissons et les coraux semblaient
visiblement à l'aise, le dosage avec de la vodka a repris, toutefois
seulement avec 7 ml. Au cours des jours suivants le système a été
suivi avec attention, mais il n'y a plus eu de turbidité. Jusqu'à
aujourd'hui cet aquarium fonctionne avec 7 ml de vodka par jour,
sans apparition de problème similaire.
Il faut noter que les
coraux étaient nettement plus clairs et que la coloration des
scléractiniaires s'était intensifiée après les deux explosions
bactériennes. Essentiellement les espèces d'Acropora brunes sont
devenues partiellement vertes, d'autres bleues.
D'autres
scléractiniaires sont également devenus plus colorés, les gorgones
et les coraux-cuir étaient visiblement plus clairs.
Afin de
réaliser le dosage de manière plus simple Michael Mrutzek s'est
décidé pour l'utilisation d'une pompe de dosage de
"Aquaristik-DosierTechnik" (ADT). Celle-ci a repris le dosage
journalier de la vodka.
Pour la reproduction des constatations
rapportées, cette méthode a été mise en oeuvre dans un autre bac.
L'opération s'est déroulée selon le schéma décrit et les paramètres
de l'eau ont été contrôlés en permanence. Dans ce cas encore plus
souvent, car la quantité de vodka dosée devait être réduite
parallèlement à la diminution de la quantité de nitrates. Au bout de
six semaines seulement, il n'y avait plus de nitrates détectables,
l'addition de vodka avait été diminuée par deux à ce moment là, ce
qui a probablement évité une explosion bactérienne. Le bac
fonctionne depuis un an avec une dose de vodka journalière de 7 ml
et aucune quantité de nitrates ne peut être détectée à l'aide des
tests disponibles.
Lors de tous ces essais aucun autre paramètre
n'a été modifié, c'est à dire pas d'augmentation de changement
d'eau, pas d'autres mesures complémentaires afin de décomposer les
nitrates ou les phosphates.
Expériences chez d'autres
aquariophiles
 Après avoir trouvé une voie de contrôle du dosage, des
amis aquariophiles ont été sollicités pour savoir s'ils désiraient
tester cette méthode. La recommandation était de doser directement
dans l'aquarium 1 ml de vodka durant les deux premiers jours,
ensuite sur la base d'un intervalle de deux jours d'augmenter à 2
ml, 3 ml et ainsi de suite jusqu'à 14 ml. Après avoir trouvé une voie de contrôle du dosage, des
amis aquariophiles ont été sollicités pour savoir s'ils désiraient
tester cette méthode. La recommandation était de doser directement
dans l'aquarium 1 ml de vodka durant les deux premiers jours,
ensuite sur la base d'un intervalle de deux jours d'augmenter à 2
ml, 3 ml et ainsi de suite jusqu'à 14 ml.
Ingo Bänsch a démarré
avec l'essai et dans ce cas également en l'espace de quatre semaines
les nitrates et les phosphates ont complètement disparu. Avant, I.
Binsch avait toujours des problèmes avec ces substances nutritives
et il songeait déjà à acquérir un filtre à nitrates. Il ne faut pas
omettre de signaler que son bac est petit (volume net environ 120
litres) et que celui-ci est certainement surpeuplé par l'un ou
l'autre poisson. Depuis longtemps il utilisait donc des adsorbeurs
de phosphates, mais qui n'ont pas été renouvelé durant l'essai.
D'autres essais ont suivi, qui se sont également déroulés de manière
positive.
 Rapidement, une autre prise de position par courriel
d'un utilisateur : "Depuis environ huit semaines je distribue
journellement de la vodka, avec une petite pause de 10 jours.
Malheureusement des tests trop âgés ont affiché des valeurs
meilleures et ainsi j'ignorais le mauvais état de mon eau. Je ne
l'ai constaté que par la croissance renforcée des algues et les
bulles d'air qui s'y rattachaient le soir. Avant la mise en oeuvre,
les valeurs de l'eau selon JBL (avec des tests plus récents) : No3
> 25 mg/1, PO4 > environ 1 mg/1, Si > 3 mg/l. J'utilise
exclusivement de l'eau de conduite, du Silicarbon et du Contraphos
(Société Aquaconnect). J'ai commencé avec 10 gouttes par jour (le
soir), augmentation de 10 gouttes chaque jour. Arrivé à 100 gouttes,
j'ai mesuré en ml. Jusqu'à 14 ml, l'eau était ensuite légèrement
trouble et les vitres montraient un dépôt bizarre. J'ai arrêté une
journée, puis j'ai continué avec 12 ml. Au bout de quatre jours les
vitres arboraient de nouveau un dépôt bizarre. La quantité de vodka
a de nouveau été réduite, d'abord à 10 ml, trois jours plus tard (de
nouveau un dépôt blanchâtre sur les vitres) à 8 ml et à présent
après encore 2 jours à 6 ml. La vodka était cependant ajoutée chaque
jour. Valeurs actuelles de l'eau (mesurées avec Salifert) : No3 =
non détectables PO4 = 0,1 mg/1 Si = 1 mg/1 Malgré les silicates
présents dans l'eau il n'y a pas de petites bulles ou algues
visqueuses visibles. La plupart des animaux se portent très bien, un
corail cuir champignon (j'en possède deux, seulement l'un présente
un comportement particulier) épanouit davantage ses polypes depuis
quelques jours. Mais ceci pourrait avoir d'autres causes, pas la
moindre idée. Toutefois mon corail-bulles ne s'ouvre plus
correctement depuis quelque temps. Y a t'il un rapport avec les
paramètres de l'eau, je ne le sais pas non plus. Et peut-être
n'apprécie t'il pas le nouvel emplacement. Sinon, tous les autres
animaux sont en pleine forme. Seules mes belles algues réduisent, ce
que je n'apprécie pas trop. C'est finalement tout ce que j'ai à dire
concernant le sujet". Rapidement, une autre prise de position par courriel
d'un utilisateur : "Depuis environ huit semaines je distribue
journellement de la vodka, avec une petite pause de 10 jours.
Malheureusement des tests trop âgés ont affiché des valeurs
meilleures et ainsi j'ignorais le mauvais état de mon eau. Je ne
l'ai constaté que par la croissance renforcée des algues et les
bulles d'air qui s'y rattachaient le soir. Avant la mise en oeuvre,
les valeurs de l'eau selon JBL (avec des tests plus récents) : No3
> 25 mg/1, PO4 > environ 1 mg/1, Si > 3 mg/l. J'utilise
exclusivement de l'eau de conduite, du Silicarbon et du Contraphos
(Société Aquaconnect). J'ai commencé avec 10 gouttes par jour (le
soir), augmentation de 10 gouttes chaque jour. Arrivé à 100 gouttes,
j'ai mesuré en ml. Jusqu'à 14 ml, l'eau était ensuite légèrement
trouble et les vitres montraient un dépôt bizarre. J'ai arrêté une
journée, puis j'ai continué avec 12 ml. Au bout de quatre jours les
vitres arboraient de nouveau un dépôt bizarre. La quantité de vodka
a de nouveau été réduite, d'abord à 10 ml, trois jours plus tard (de
nouveau un dépôt blanchâtre sur les vitres) à 8 ml et à présent
après encore 2 jours à 6 ml. La vodka était cependant ajoutée chaque
jour. Valeurs actuelles de l'eau (mesurées avec Salifert) : No3 =
non détectables PO4 = 0,1 mg/1 Si = 1 mg/1 Malgré les silicates
présents dans l'eau il n'y a pas de petites bulles ou algues
visqueuses visibles. La plupart des animaux se portent très bien, un
corail cuir champignon (j'en possède deux, seulement l'un présente
un comportement particulier) épanouit davantage ses polypes depuis
quelques jours. Mais ceci pourrait avoir d'autres causes, pas la
moindre idée. Toutefois mon corail-bulles ne s'ouvre plus
correctement depuis quelque temps. Y a t'il un rapport avec les
paramètres de l'eau, je ne le sais pas non plus. Et peut-être
n'apprécie t'il pas le nouvel emplacement. Sinon, tous les autres
animaux sont en pleine forme. Seules mes belles algues réduisent, ce
que je n'apprécie pas trop. C'est finalement tout ce que j'ai à dire
concernant le sujet".
(Fin de la citation)
La
théorie
Afin de pouvoir soutenir par la théorie les données
expérimentales présentées, des recherches littéraires ont été
entreprises, avec l'espoir, de trouver des données scientifiques
concernant la croissance des bactéries et de leur influence sur la
quantité de nitrates et de phosphates dans l'eau. Ce faisant les
moteurs de recherche ont trouvé une profusion d'articles
scientifiques et de résumés d'articles à propos d'un sujet sûrement
très intéressant pour les aquariophiles :
Polyphosphat-Akkumulierende Bakterien (PAB = bactéries accumulant
les polyphosphates).
Dans le traitement des eaux usées on
utilise depuis plus de 30 ans le dénommé : "Enhanced Biological
Phosphorus Removal" (EPBR = élimination biologique accrue des
phosphates) (Crocetti et al. 1999). Ceci est d'autant plus étonnant
que ni la littérature aquariophile américaine ou allemande n'ont
jamais rien publié à ce sujet. Uniquement sur internet sur une
Homepage non commerciale (voir pages Internet dans Littérature en
fin d'article) j'ai trouvé un article du Dr. Gerd Kassebeer, qui à
l'origine a paru dans la revue « Aquarium Heute » et dans lequel il
est question de bactéries, qui peuvent accumuler des phosphates dans
leurs cellules (Kassebeer 1995).
Bactéries accumulatrices
de phosphates
Il s'agit d'un groupe de différentes
bactéries, qui se ressemblent en ce que en dépendance de diverses
conditions anaérobies ou aérobies de milieu et de la présence de
composés de carbone organique elles accumulent et libèrent de
nouveau des phosphates inorganiques (Mino 1999). Ce que ces
bactéries hétérotrophes effectuent finalement, consiste à absorber
de l'eau des composés de carbone organique sous un manque d'oxygène
et à rendre en même temps des phosphates dans l'eau. Ces phosphates
proviennent de la décomposition de polyphosphates (PolyP) riches en
énergie, l'énergie libérée étant utilisée à l'absorption de carbone
organique. Le tout n'est pas véritablement excitant d'un point de
vue aquariophile, car nous souhaitons aboutir à une élimination des
phosphates et non à une émission de phosphates. En effet ceci ne
constitue que la première partie de l'histoire, car les bactéries
similaires peuvent brûler ces composés de carbone organique afin
d'obtenir de l'énergie dans une phase aérobie s'ajoutant à la phase
anaérobie et absorber en même temps des phosphates inorganiques. Et
de façon caractéristique, elles absorbent ce faisant plus de
phosphates qu'elles n'en ont libéré avant.
Capacités
maximales de décomposition ?
Afin d'avoir une idée, de
quelles capacités de décomposition il est question, les recherches
ont été poursuivies et en définitive nous avons trouvé une
publication de Crocetti et al. (2000), qui nous a renseigné. Un
document, qui y est publié, fournit des données, qui prouvent que
lors d'une charge finale de phosphates de 57 mg/l PO4-P (soit 174,7
mg/l PO4) et une quantité d'acétate dans l'eau de 309 mg/l, la
quantité de PO4 après le passage de la phase anaérobie (et la
libération de phosphates par les bactéries qui s'en suit) monte à
144 mg/l PO4- P (soit 441,3 mg/l de PO4.
L'eau usée est ensuite
ressortie du filtre après passage dans la phase aérobie (au cours de
laquelle des phosphates sont accumulés) avec 0,05 mg/l de PO4-P
(soit 0,15 mg/l de PO4) et sans acétate détectable. Ceci, avec une
diminution de la quantité de phosphates de 1/1000 de la charge
finale, est vraiment excitant !
Naturellement nous ne pouvons
pas transposer cela à nos aquariums et en outre les auteurs parlent
avec une certaine fierté d'une boue de décantation de grande
efficacité éliminant les phosphates, qui à la fin pouvait produire
une quantité de phosphore équivalent à 15 % de biomasse totale.
Comme dit nous ne pouvons utiliser ces données. A intervalles
réguliers le matériau de filtration chargé de bactéries est échangé
après la phase oxique et en fin de compte les phosphates éliminés du
système.
Définition des PAB
 Le désaccord règne à ce sujet, à savoir quelles bactéries
sont impliquées ou lesquelles conviennent le mieux lors de l'EPBR.
Mino (2000) donne un aperçu concernant les différerents groupes
potentiels et participants de bactéries, parmi lesquels
Acinetobacter spp., Microlunatus phosphovorus,
Lampropedia spp. et des espèces du genre Rhodocytus.
Diverses autres publications s'expliquent spécialement sur ce sujet
(Lee et al . 2002, Levantsi et al. 2002, Onuki et al. 2002, Bond et
al. 1999, Sidat et al. 1999). Une bactérie du groin ß-Proteobacteria
a été identifiée PAB et dénommée comme "Candidatus Accumulibacter
phosphatis" (Blackall et al. 2002, Zeng et al. 2003). De plus il a
pu être constaté chez Paracoccus denitrificans, que ces
bactéries peuvent éliminer en même temps des phosphates et des
nitrates et cela indépendamment même des situations variables
oxiques et anoxiques (Barak & van Rijm 2000). P.
denitrificans entrerait donc principalement en fonction comme
organisme clé dans l'expérimentation à base de vodka. En plus P.
denitrificans représente un dénitrificateur typique (Schlegel
1992), qui ne manque pas dans nos aquariums en tant que souche
naturelle dans les pierres vivantes. Le désaccord règne à ce sujet, à savoir quelles bactéries
sont impliquées ou lesquelles conviennent le mieux lors de l'EPBR.
Mino (2000) donne un aperçu concernant les différerents groupes
potentiels et participants de bactéries, parmi lesquels
Acinetobacter spp., Microlunatus phosphovorus,
Lampropedia spp. et des espèces du genre Rhodocytus.
Diverses autres publications s'expliquent spécialement sur ce sujet
(Lee et al . 2002, Levantsi et al. 2002, Onuki et al. 2002, Bond et
al. 1999, Sidat et al. 1999). Une bactérie du groin ß-Proteobacteria
a été identifiée PAB et dénommée comme "Candidatus Accumulibacter
phosphatis" (Blackall et al. 2002, Zeng et al. 2003). De plus il a
pu être constaté chez Paracoccus denitrificans, que ces
bactéries peuvent éliminer en même temps des phosphates et des
nitrates et cela indépendamment même des situations variables
oxiques et anoxiques (Barak & van Rijm 2000). P.
denitrificans entrerait donc principalement en fonction comme
organisme clé dans l'expérimentation à base de vodka. En plus P.
denitrificans représente un dénitrificateur typique (Schlegel
1992), qui ne manque pas dans nos aquariums en tant que souche
naturelle dans les pierres vivantes.
Quelles sources de
carbone conviennent pour les PAB ?
Il est clairement
démontré dans cet article que l'éthanol constitue une forme de
carbone organique convenable et facilement accessible, afin de
diminuer efficacement la quantité de nitrates et de phosphates dans
l'aquarium. Dans la littérature il est par contre écrit que les PAB
absorbent de préférence des acides gras à chaîne courte comme
l'acétate ou le propionate et les métabolisent (Mino 2000, van Niel
et al. 1998). L'acétate, l'anion de l'acide acétique, est également
utilisé en aquariophilie récifale outre l'alcool, afin de renforcer
la croissance des bactéries de filtration.
Comme Barak et van
Rijn (2000) ont pu le montrer, P. denitrificans est une
bactérie hétérotrophe anaérobie facultative, qui lors d'un manque
d'oxygène commute sur un métabolisme anaérobie et utilise les
nitrates à la place de l'oxygène comme récepteur d'électrons et
dénitrifie celui-ci. La bactérie doit être nourrie avec une source
de carbone. En opposition à la dénitrification l'accumulation des
phosphates se produit aussi dans le milieu oxygéné, à la condition
de disposer d'une source convenable suffisante de carbone (dans ce
cas il est question d'acétate). Il est possible de décomposer dans
l'aquarium aussi bien des nitrates que des phosphates avec ce petit
organisme. Il faut insister sur le fait qu'en ce qui concerne P.
denitrificans il ne s'agit pas d'une PAB, car elle ne présente
pas les caractéristiques physiologiques typiques d'une PAB, comme
par exemple un changement obligatoire entre phase oxique et
anoxique.
Les bactéries accumulant les polyphosphates ne
sont pas présentes dans nos aquariums ou nous ne pouvons pas leur
offrir les conditions environnementales, afin que leurs propriétés
puissent être utiles pour nous. Il s'agit toutefois d'un sujet que
nous ne devons pas perdre de vue d'un point de vue aquariophile. Par
contre Paracoccus denitrificans constitue un candidat
convenable, afin de pouvoir expliquer, ce qui s'est passé lors des
expérimentations avec la vodka. Finalement cette bactérie
hétérotrophe est nourrie avec de l'éthanol et décompose les nitrates
dans les zones anaérobies des sédiments et des pierres vivantes,
simultanément elle absorbe des phosphates présents dans
l'environnement. En présence de problèmes de nitrates et de
phosphites il ne faut pas, d'après les expériences rapportées ici,
obligatoirement recourir à la technique. Il suffit d'offrir une
source de carbone aux bactéries hétérotrophes présentes dans les
pierres vivantes et le substrat. Etant donné qu'il se produit
également par le dosage de l'éthanol une chute significative de la
quantité de phosphates, est également très intéressant. Comme dit la
croissance de tous les organismes nécessite l'élément nutritif
phosphore.
 Lorsque les bactéries se développent tellement qu'elles
forment déjà des dépôts mucosiques sur les vitres et la décoration,
il ne doit alors pas être étonnant que la quantité de phosphate
diminue nettement. Les biofilms ne peuvent pas épaissir à l'infini.
A partir d'un certain point, des parties se détachent et une
nouvelle couche pousse, jusqu'à ce que celle-ci soit à son tour
arrachée par le courant (Hûster 1996). Un écumage efficace
récupérera les restes de bactéries mortes et retirera ainsi
définitivement le phosphore du système. Sinon il se produirait de
nouveau une augmentation de la quantité de phosphates. Même si le
phosphate organique n'est plus transformé dans les bactéries en
phosphate inorganique – ce qui signifie, que nous ne pouvons pas le
mesurer – nous pourrions certainement conclure de la présence du
phosphore dans le bac par une croissance couronnée de succès des
algues et un nouvel assombrissement du tissu des coraux. Mais comme
décrit ce n'était pas le cas. C'est pour cette raison que le
récipient de collecte de l'écumeur constitue un composant important
de l'aquarium, sans lequel le retrait des phosphates ne
fonctionnerait certainement pas. Une quantité nettement plus
importante d'adsorbat dans le récipient de collecte de l'écumeur a
été constatée lors de l'utilisation de la méthode à base de vodka.
Sans doute ceci ne constitue qu'un revers de la médaille. Même si
par élimination des nitrates et des phosphates de meilleures
conditions environnementales se créent, ceci n'explique pas encore
l'énorme expansion et la croissance renforcée des polypes des
coraux. Il existe de nombreux aquariums, qui d'une part peuvent
présenter de faibles quantités de substances nutritives, mais où les
coraux ne croissent pas obligatoirement plus vite ou ne vont pas
mieux dans l'ensemble. Lorsque les bactéries se développent tellement qu'elles
forment déjà des dépôts mucosiques sur les vitres et la décoration,
il ne doit alors pas être étonnant que la quantité de phosphate
diminue nettement. Les biofilms ne peuvent pas épaissir à l'infini.
A partir d'un certain point, des parties se détachent et une
nouvelle couche pousse, jusqu'à ce que celle-ci soit à son tour
arrachée par le courant (Hûster 1996). Un écumage efficace
récupérera les restes de bactéries mortes et retirera ainsi
définitivement le phosphore du système. Sinon il se produirait de
nouveau une augmentation de la quantité de phosphates. Même si le
phosphate organique n'est plus transformé dans les bactéries en
phosphate inorganique – ce qui signifie, que nous ne pouvons pas le
mesurer – nous pourrions certainement conclure de la présence du
phosphore dans le bac par une croissance couronnée de succès des
algues et un nouvel assombrissement du tissu des coraux. Mais comme
décrit ce n'était pas le cas. C'est pour cette raison que le
récipient de collecte de l'écumeur constitue un composant important
de l'aquarium, sans lequel le retrait des phosphates ne
fonctionnerait certainement pas. Une quantité nettement plus
importante d'adsorbat dans le récipient de collecte de l'écumeur a
été constatée lors de l'utilisation de la méthode à base de vodka.
Sans doute ceci ne constitue qu'un revers de la médaille. Même si
par élimination des nitrates et des phosphates de meilleures
conditions environnementales se créent, ceci n'explique pas encore
l'énorme expansion et la croissance renforcée des polypes des
coraux. Il existe de nombreux aquariums, qui d'une part peuvent
présenter de faibles quantités de substances nutritives, mais où les
coraux ne croissent pas obligatoirement plus vite ou ne vont pas
mieux dans l'ensemble.
Comment se produit une croissance
améliorée ?
 Suite à l'importante multiplication des bactéries par le
dosage d'éthanol, plus de bactéries sont extraites des biofilms et
se trouvent en liberté dans l'eau. Une partie de ces particules sont
rapidement écumées, mais une partie sert aussi de nourriture aux
coraux. La vigueur de l'expansion des polypes peut (mais ne doit
pas) indiquer une acquisition de nourriture. En règle générale
l'expansion des polypes comme chez les scléractiniaires durant la
phase nocturne est, lorsque la micro-faune et le zooplancton sortent
des pierres vivantes, nettement plus importante que durant le jour. Suite à l'importante multiplication des bactéries par le
dosage d'éthanol, plus de bactéries sont extraites des biofilms et
se trouvent en liberté dans l'eau. Une partie de ces particules sont
rapidement écumées, mais une partie sert aussi de nourriture aux
coraux. La vigueur de l'expansion des polypes peut (mais ne doit
pas) indiquer une acquisition de nourriture. En règle générale
l'expansion des polypes comme chez les scléractiniaires durant la
phase nocturne est, lorsque la micro-faune et le zooplancton sortent
des pierres vivantes, nettement plus importante que durant le jour.
Une autre explication veut que nous mettions à la disposition
des bactéries hétérotrophes, vivant dans le mucus des coraux, une
source complémentaire de nourriture avec l'éthanol, ce qui
probablement fait que les populations de bactéries poussent plus
rapidement dans le mucus des coraux. Lorsque le corail peut de
nouveau digérer lui-même son propre mucus (ce qui est douteux), leur
spectre alimentaire se trouverait ainsi élargi.
Depuis plusieurs
années déjà le mucus des coraux attire l'attention de la recherche
biologique en tant que biofilm. Il est de plus en plus sûr que la
multiplicité des diverses bactéries, qui y vivent, ont d'une
certaine façon une interaction avec le corail même. Assurément il
n'est pas sûr de pouvoir déjà parler d'une symbiose, trop peu de
données expérimentales concernant ce sujet sont disponibles.
Pas de limitation des substances nutritives par retrait
sélectif
Avec la forme présentée de dosage de l'éthanol au
moyen de la vodka il est possible de décomposer aussi bien les
nitrates que les phosphates. L'avantage consiste à ne pas créer de
limitation des substances nutritives en réduisant simultanément les
deux substances nutritives, laquelle peut par exemple se produire
lorsqu'on retire uniquement des phosphates avec un adsorbeur ou un
fixateur liquide des phosphates ou uniquement des nitrates avec un
filtre dénitrateur traditionnel. Il ne s'agit donc pas seulement
d'une méthode simple mais également sûre.
Il convient de
recommander, d'ajouter chaque jour de faibles quantités de vodka
directement dans l'aquarium. Il est certainement difficile, de
donner une méthode de dosage recommandée universellement valable,
car les aquariums sont tous différents. Nous considérons comme sensé
de commencer le dosage avec 0,5 ml de vodka chaque jour par tranche
de 100 litres d'eau de l'aquarium (volume net) pour les deux
premiers jours, 1 ml/100l pour le troisième et le quatrième jour et
2 ml/100l jusqu'au septième jour inclus.
 Au plus tard à ce moment là, il faut commencer le
contrôle régulier de la quantité de nitrates et de phosphates.
Justement dans de très petits bacs avec un volume net de 100 à 200
litres la limite supérieure peut déjà être atteinte. Dans les
aquariums plus grands il est possible d'augmenter la quantité de
vodka d'1 ml chaque fois, à intervalle de trois jours. La chute de
la quantité de nitrates et de phosphates sert d'indicateur pour la
croissance des populations de bactéries. La quantité de phosphates
reflète surtout la croissance de toutes les bactéries hétérotrophes,
tandis que la décomposition des nitrates ne peut finalement
concerner qu'un rapport concernant les dénitrificateurs. Un bon test
phosphates ne doit pas manquer lors de l'utilisation de cette
méthode. Au plus tard à ce moment là, il faut commencer le
contrôle régulier de la quantité de nitrates et de phosphates.
Justement dans de très petits bacs avec un volume net de 100 à 200
litres la limite supérieure peut déjà être atteinte. Dans les
aquariums plus grands il est possible d'augmenter la quantité de
vodka d'1 ml chaque fois, à intervalle de trois jours. La chute de
la quantité de nitrates et de phosphates sert d'indicateur pour la
croissance des populations de bactéries. La quantité de phosphates
reflète surtout la croissance de toutes les bactéries hétérotrophes,
tandis que la décomposition des nitrates ne peut finalement
concerner qu'un rapport concernant les dénitrificateurs. Un bon test
phosphates ne doit pas manquer lors de l'utilisation de cette
méthode.
Dès que des dépôts de bactéries deviennent visibles sur
les vitres et la décoration, il faut réduire le dosage et certes
d'environ un tiers par rapport à la quantité actuelle. Afin
d'empêcher un probable écroulement des populations bactériennes il
est conseillé de ne pas arrêter complètement le dosage, mais de
continuer à travailler avec des quantités journalières plus faibles.
Un contrôle régulier des paramètres, particulièrement de la quantité
de nitrates et de phosphates est très important. Dès qu'il n'y a
plus nitrates détectables, il faut diminuer la dose d'un tiers ou
même de la moitié. Pour les dénitrificateurs les nitrates deviennent
le facteur limitant et la croissance des bactéries se ralentit,
raison pour laquelle le dosage du carbone doit également être
diminué. Trop de carbone favorise alors probablement la croissance
d'autres bactéries hétérotrophes, qui deviennent visibles sous la
forme de dépôts nuicosiques. Une concurrence entre les dénitrifiants
et d'autres bactéries hétérotrophes ne peut être exclue.
Précaution particulière dans le cas de bacs anciens
Une attention particulière doit être portée aux bacs âgés,
dans lesquels au fil des années des quantités élevées de substances
nutritives ont été mesurées, car aussi bien les coraux que les
algues et les bactéries se sont acclimatés à ce milieu. Avec le
dosage de la vodka il y a une intervention brutale dans le système
et indépendamment de cela, que cette mesure soit évaluée
positivement ou négativement, les organismes doivent s'y adapter.
Dans de tels aquariums l'augmentation du dosage de vodka doit se
dérouler très lentement durant six à neuf mois et avec de longs
intervalles entre les augmentations, afin de ne pas subir de pertes.
Là aussi le contrôle de la quantité de substances nutritives est
très important.
Conclusion
Il ne faut pas
oublier, que cette méthode à base de vodka ne retire certainement
pas que des nitrates et des phosphates du système, mais a un effet
positif sur l'alimentation et ainsi sur la croissance des coraux. Il
ne s'agit donc pas seulement d'une méthode pour les aquariums à
problème, mais elle peut absolument être utilisée dans des aquariums
non chargés, bien sûr en dosage plus faible. Pour cela il faut que
l'aquariophile définisse lui-même la mesure idéale à partir de la
dose proposée au départ de 1ml/100 l.
NDLR : Cette méthode
d'élimination des nitrates et des phosphates a soulevé les passions
en Allemagne. Si certains aquariophiles ont vu l'emploi de la
méthode couronnée de succès quelques uns ont eu des échecs partiel
dus à des raisons difficiles à déterminer. Cette méthode doit être
utilisé avec toutes les précautions qui s'imposent telles que
décrites dans l'article. En aucun cas les auteurs ne pourraient être
tenus pour responsables en cas de pertes d'animaux liées à
l'utilisation de cette méthode. Il est prévu la publication d'un
autre article concernant cette méthode de la part d'un autre auteur.
Avec l'aimable
autorisation de M. Michael Mrutzek et Jörg Kokott
Littérature
- Karak, Y ; A. & Van Rijm, J. (2000), Atypical
polyphosphate accumulation by the denitrifying bacterium Paracoccus
denitrificans. Applied and Environmental Microbiology 66: 1209-1212.
- Blackall, L. L., Crocetti, G. R. Saunders, A. M. & Bond,
P. L. (2002): A review and update of the microbiology of enhanced
biological phosphorus removal in wastewater treatment plants.
Antonie Van Leeuwenhoek 81 : 681-691.
- Bond, P. L., Erhart, R.,
Wagner, M., J. & Blackall L. l. (1999): Identification of some
of the major groups of bacteria in efficient and non efficient
biological phosphorus removal activated sludge systems. Applied and
Environmental Microbiology 65: 4077-4084.
- Crocetti, G. R.,
Hugenholtz, P., Bond, P. l., Schuler, A., Keller, J., Jenkins, D.
& Blackall, L. l., (2000): Identification of
Plyphosphate-Accumulating Organisms and Design of 16S rRNA- Directed
Probes for their Detection and Quantation. Applied and Environmental
Microbiology 66: 1175-1182.
- Hüster, R., (2003): Biofilme,
geniale Erfindung der Natur. 6. Internationales
Meerwasser-Symposium, Bochum. S 27-35.
- Kassebeer, G., (1995):
Ist unser Aquarium eine Kläranlage ? Aquarium Hute 13 (2): 100-118.
- Lee, T. J., Kawaharasaki, M., Matsummara, M., & Nakamura,
K. (2002): Microbila community structures of activated sludges
dominated with polyphosphate-accumulating bacteria and
glycogen-accumulating bacteria. Environmental Technology 23:
747-755.
- Levantesi, C., Serafim, L. S., Crocetti, G. R.,
Lemos, P. C., Rossetti, S., Blackall, L. L., & reis, M. A.
(2002) : Analysis of the microbial community structure and fonction
of a laboratory scale enhanced biological phosphorus removal
reactor. Environmental Microbiology 4: 559-669.
- Mino, T.,
(2000) : Microbial selection of polyphosphate-accumulating bacteria
in activated sludge wastewater treatment process for enhanced
biological phosphate removal. Journal of Biochemistry - Tokyo 65:
341-348.
- Onuki, M., Satoh, H. & Mino, T. (2002): Analysis
of microbial community that performs enhanced biological phosphorus
removal in activated sludge fed with acetate. Water Science and
Technology 46: 145-153.
- Schlegel, H. G. (1992): Allgemeine
Mikrobiologie. 7. Aufl., Thieme Verlag, Stuttgart.
- Sidat, M.,
Bux, F., & Kasan, H. C., Zehnder, A. J. B. & Kortstee, G.,
J., J. (1998): Inhibition of anaerobic phosphate release by nitric
oxide in activayed sludge. Applied and Environmental Microbiology
64: 2925-2930.
- Zeng, R., Saunders, A. M., Yan, Z., Blackall,
L. L. & Keller, J. (2003): Identification and comparison of
aerobic and denitrifying polyphosphate accumulating organisms.
Biotechnology and Bioengineering 83: 140-148.
http:/www.deters-ing.de/ gastbeitraegelklaeranlage.htm
| | | | | |
| |
|
© RECIF FRANCE - Tous
droits réservés. Récif onLine V3.0
Association Française des
Amateurs d'Aquariophilie Marine et Récifale.
Editeur
des Lettres
Récifales, seule publication
bimestrielle de langue française consacrée exclusivement à
l'aquariophilie marine et
récifale.
Mentions légales
|


 Depuis des décennies nous essayons d'améliorer les
conditions de maintenance de nos coraux et de nos poissons. De
nouveaux articles parlent de progrès, de nouvelles techniques et de
moyens qui doivent nous permettre d'améliorer la qualité de vie de
nos pensionnaires. Depuis plus de deux ans l'un des auteurs (Michael
Mrutzek) travaille sur une méthode, afin d'améliorer la dégradation
des importantes quantités de nitrates dans les aquariums d'eau de
mer et par là même les conditions de vie des animaux d'aquarium. Les
enseignements récoltés sont relatés et étayés par des connaissances
théoriques.
Depuis des décennies nous essayons d'améliorer les
conditions de maintenance de nos coraux et de nos poissons. De
nouveaux articles parlent de progrès, de nouvelles techniques et de
moyens qui doivent nous permettre d'améliorer la qualité de vie de
nos pensionnaires. Depuis plus de deux ans l'un des auteurs (Michael
Mrutzek) travaille sur une méthode, afin d'améliorer la dégradation
des importantes quantités de nitrates dans les aquariums d'eau de
mer et par là même les conditions de vie des animaux d'aquarium. Les
enseignements récoltés sont relatés et étayés par des connaissances
théoriques.  Il ne faut pas oublier le filtre à nitrates basé sur
le soufre qui a vu le jour ces dernières années. Tous les systèmes
décrits jusqu'à présent hébergent des dénitrificateurs
hétérotrophes, ce qui signifie, que contrairement aux plantes ils ne
peuvent pas créer eux-mêmes leur nourriture par utilisation de
l'énergie solaire, mais qu'ils doivent manger de façon active. Dans
le filtre sur soufre les dénitrificateurs autotrophes croissent par
contre, n'utilisant certes pas la lumière solaire, mais l'énergie
provenant de l'oxydation du soufre élémentaire. Les bactéries n'ont
pas besoin d'être nourries. Lors de l'oxydation du soufre
élémentaire les bactéries produisent de l'acide sulfurique (H2SO4),
qui est neutralisé dans une colonne de calcaire installée en sortie.
D'une part le filtre sur soufre permet une dégradation des nitrates,
d'autre part il fonctionne comme un réacteur à calcaire, ce qui peut
mener à des problèmes de quantité de calcium et de dureté
carbonatée.
Il ne faut pas oublier le filtre à nitrates basé sur
le soufre qui a vu le jour ces dernières années. Tous les systèmes
décrits jusqu'à présent hébergent des dénitrificateurs
hétérotrophes, ce qui signifie, que contrairement aux plantes ils ne
peuvent pas créer eux-mêmes leur nourriture par utilisation de
l'énergie solaire, mais qu'ils doivent manger de façon active. Dans
le filtre sur soufre les dénitrificateurs autotrophes croissent par
contre, n'utilisant certes pas la lumière solaire, mais l'énergie
provenant de l'oxydation du soufre élémentaire. Les bactéries n'ont
pas besoin d'être nourries. Lors de l'oxydation du soufre
élémentaire les bactéries produisent de l'acide sulfurique (H2SO4),
qui est neutralisé dans une colonne de calcaire installée en sortie.
D'une part le filtre sur soufre permet une dégradation des nitrates,
d'autre part il fonctionne comme un réacteur à calcaire, ce qui peut
mener à des problèmes de quantité de calcium et de dureté
carbonatée. 
 Après qu'avec 15 ml/jour aucun effet secondaire négatif
n'a été constaté, l'augmentation à 16 ml a été effectuée ce qui a eu
comme suite que le jour suivant une légère turbidité de l'eau a été
constatée et qu'un dépôt mucosique recouvrait les vitres et la
décoration. Dès ce moment l'écumeur a été immédiatement accéléré et
l'additif de vodka arrêtée. Le lendemain la turbidité était encore
reconnaissable et le dépôts mucosique encore présent, mais plus
aussi important que la veille. 24 heures plus tard tout avait
disparu.
Après qu'avec 15 ml/jour aucun effet secondaire négatif
n'a été constaté, l'augmentation à 16 ml a été effectuée ce qui a eu
comme suite que le jour suivant une légère turbidité de l'eau a été
constatée et qu'un dépôt mucosique recouvrait les vitres et la
décoration. Dès ce moment l'écumeur a été immédiatement accéléré et
l'additif de vodka arrêtée. Le lendemain la turbidité était encore
reconnaissable et le dépôts mucosique encore présent, mais plus
aussi important que la veille. 24 heures plus tard tout avait
disparu.  Après avoir trouvé une voie de contrôle du dosage, des
amis aquariophiles ont été sollicités pour savoir s'ils désiraient
tester cette méthode. La recommandation était de doser directement
dans l'aquarium 1 ml de vodka durant les deux premiers jours,
ensuite sur la base d'un intervalle de deux jours d'augmenter à 2
ml, 3 ml et ainsi de suite jusqu'à 14 ml.
Après avoir trouvé une voie de contrôle du dosage, des
amis aquariophiles ont été sollicités pour savoir s'ils désiraient
tester cette méthode. La recommandation était de doser directement
dans l'aquarium 1 ml de vodka durant les deux premiers jours,
ensuite sur la base d'un intervalle de deux jours d'augmenter à 2
ml, 3 ml et ainsi de suite jusqu'à 14 ml.  Rapidement, une autre prise de position par courriel
d'un utilisateur : "Depuis environ huit semaines je distribue
journellement de la vodka, avec une petite pause de 10 jours.
Malheureusement des tests trop âgés ont affiché des valeurs
meilleures et ainsi j'ignorais le mauvais état de mon eau. Je ne
l'ai constaté que par la croissance renforcée des algues et les
bulles d'air qui s'y rattachaient le soir. Avant la mise en oeuvre,
les valeurs de l'eau selon JBL (avec des tests plus récents) : No3
> 25 mg/1, PO4 > environ 1 mg/1, Si > 3 mg/l. J'utilise
exclusivement de l'eau de conduite, du Silicarbon et du Contraphos
(Société Aquaconnect). J'ai commencé avec 10 gouttes par jour (le
soir), augmentation de 10 gouttes chaque jour. Arrivé à 100 gouttes,
j'ai mesuré en ml. Jusqu'à 14 ml, l'eau était ensuite légèrement
trouble et les vitres montraient un dépôt bizarre. J'ai arrêté une
journée, puis j'ai continué avec 12 ml. Au bout de quatre jours les
vitres arboraient de nouveau un dépôt bizarre. La quantité de vodka
a de nouveau été réduite, d'abord à 10 ml, trois jours plus tard (de
nouveau un dépôt blanchâtre sur les vitres) à 8 ml et à présent
après encore 2 jours à 6 ml. La vodka était cependant ajoutée chaque
jour. Valeurs actuelles de l'eau (mesurées avec Salifert) : No3 =
non détectables PO4 = 0,1 mg/1 Si = 1 mg/1 Malgré les silicates
présents dans l'eau il n'y a pas de petites bulles ou algues
visqueuses visibles. La plupart des animaux se portent très bien, un
corail cuir champignon (j'en possède deux, seulement l'un présente
un comportement particulier) épanouit davantage ses polypes depuis
quelques jours. Mais ceci pourrait avoir d'autres causes, pas la
moindre idée. Toutefois mon corail-bulles ne s'ouvre plus
correctement depuis quelque temps. Y a t'il un rapport avec les
paramètres de l'eau, je ne le sais pas non plus. Et peut-être
n'apprécie t'il pas le nouvel emplacement. Sinon, tous les autres
animaux sont en pleine forme. Seules mes belles algues réduisent, ce
que je n'apprécie pas trop. C'est finalement tout ce que j'ai à dire
concernant le sujet".
Rapidement, une autre prise de position par courriel
d'un utilisateur : "Depuis environ huit semaines je distribue
journellement de la vodka, avec une petite pause de 10 jours.
Malheureusement des tests trop âgés ont affiché des valeurs
meilleures et ainsi j'ignorais le mauvais état de mon eau. Je ne
l'ai constaté que par la croissance renforcée des algues et les
bulles d'air qui s'y rattachaient le soir. Avant la mise en oeuvre,
les valeurs de l'eau selon JBL (avec des tests plus récents) : No3
> 25 mg/1, PO4 > environ 1 mg/1, Si > 3 mg/l. J'utilise
exclusivement de l'eau de conduite, du Silicarbon et du Contraphos
(Société Aquaconnect). J'ai commencé avec 10 gouttes par jour (le
soir), augmentation de 10 gouttes chaque jour. Arrivé à 100 gouttes,
j'ai mesuré en ml. Jusqu'à 14 ml, l'eau était ensuite légèrement
trouble et les vitres montraient un dépôt bizarre. J'ai arrêté une
journée, puis j'ai continué avec 12 ml. Au bout de quatre jours les
vitres arboraient de nouveau un dépôt bizarre. La quantité de vodka
a de nouveau été réduite, d'abord à 10 ml, trois jours plus tard (de
nouveau un dépôt blanchâtre sur les vitres) à 8 ml et à présent
après encore 2 jours à 6 ml. La vodka était cependant ajoutée chaque
jour. Valeurs actuelles de l'eau (mesurées avec Salifert) : No3 =
non détectables PO4 = 0,1 mg/1 Si = 1 mg/1 Malgré les silicates
présents dans l'eau il n'y a pas de petites bulles ou algues
visqueuses visibles. La plupart des animaux se portent très bien, un
corail cuir champignon (j'en possède deux, seulement l'un présente
un comportement particulier) épanouit davantage ses polypes depuis
quelques jours. Mais ceci pourrait avoir d'autres causes, pas la
moindre idée. Toutefois mon corail-bulles ne s'ouvre plus
correctement depuis quelque temps. Y a t'il un rapport avec les
paramètres de l'eau, je ne le sais pas non plus. Et peut-être
n'apprécie t'il pas le nouvel emplacement. Sinon, tous les autres
animaux sont en pleine forme. Seules mes belles algues réduisent, ce
que je n'apprécie pas trop. C'est finalement tout ce que j'ai à dire
concernant le sujet". Le désaccord règne à ce sujet, à savoir quelles bactéries
sont impliquées ou lesquelles conviennent le mieux lors de l'EPBR.
Mino (2000) donne un aperçu concernant les différerents groupes
potentiels et participants de bactéries, parmi lesquels
Acinetobacter spp., Microlunatus phosphovorus,
Lampropedia spp. et des espèces du genre Rhodocytus.
Diverses autres publications s'expliquent spécialement sur ce sujet
(Lee et al . 2002, Levantsi et al. 2002, Onuki et al. 2002, Bond et
al. 1999, Sidat et al. 1999). Une bactérie du groin ß-Proteobacteria
a été identifiée PAB et dénommée comme "Candidatus Accumulibacter
phosphatis" (Blackall et al. 2002, Zeng et al. 2003). De plus il a
pu être constaté chez Paracoccus denitrificans, que ces
bactéries peuvent éliminer en même temps des phosphates et des
nitrates et cela indépendamment même des situations variables
oxiques et anoxiques (Barak & van Rijm 2000). P.
denitrificans entrerait donc principalement en fonction comme
organisme clé dans l'expérimentation à base de vodka. En plus P.
denitrificans représente un dénitrificateur typique (Schlegel
1992), qui ne manque pas dans nos aquariums en tant que souche
naturelle dans les pierres vivantes.
Le désaccord règne à ce sujet, à savoir quelles bactéries
sont impliquées ou lesquelles conviennent le mieux lors de l'EPBR.
Mino (2000) donne un aperçu concernant les différerents groupes
potentiels et participants de bactéries, parmi lesquels
Acinetobacter spp., Microlunatus phosphovorus,
Lampropedia spp. et des espèces du genre Rhodocytus.
Diverses autres publications s'expliquent spécialement sur ce sujet
(Lee et al . 2002, Levantsi et al. 2002, Onuki et al. 2002, Bond et
al. 1999, Sidat et al. 1999). Une bactérie du groin ß-Proteobacteria
a été identifiée PAB et dénommée comme "Candidatus Accumulibacter
phosphatis" (Blackall et al. 2002, Zeng et al. 2003). De plus il a
pu être constaté chez Paracoccus denitrificans, que ces
bactéries peuvent éliminer en même temps des phosphates et des
nitrates et cela indépendamment même des situations variables
oxiques et anoxiques (Barak & van Rijm 2000). P.
denitrificans entrerait donc principalement en fonction comme
organisme clé dans l'expérimentation à base de vodka. En plus P.
denitrificans représente un dénitrificateur typique (Schlegel
1992), qui ne manque pas dans nos aquariums en tant que souche
naturelle dans les pierres vivantes.  Lorsque les bactéries se développent tellement qu'elles
forment déjà des dépôts mucosiques sur les vitres et la décoration,
il ne doit alors pas être étonnant que la quantité de phosphate
diminue nettement. Les biofilms ne peuvent pas épaissir à l'infini.
A partir d'un certain point, des parties se détachent et une
nouvelle couche pousse, jusqu'à ce que celle-ci soit à son tour
arrachée par le courant (Hûster 1996). Un écumage efficace
récupérera les restes de bactéries mortes et retirera ainsi
définitivement le phosphore du système. Sinon il se produirait de
nouveau une augmentation de la quantité de phosphates. Même si le
phosphate organique n'est plus transformé dans les bactéries en
phosphate inorganique – ce qui signifie, que nous ne pouvons pas le
mesurer – nous pourrions certainement conclure de la présence du
phosphore dans le bac par une croissance couronnée de succès des
algues et un nouvel assombrissement du tissu des coraux. Mais comme
décrit ce n'était pas le cas. C'est pour cette raison que le
récipient de collecte de l'écumeur constitue un composant important
de l'aquarium, sans lequel le retrait des phosphates ne
fonctionnerait certainement pas. Une quantité nettement plus
importante d'adsorbat dans le récipient de collecte de l'écumeur a
été constatée lors de l'utilisation de la méthode à base de vodka.
Sans doute ceci ne constitue qu'un revers de la médaille. Même si
par élimination des nitrates et des phosphates de meilleures
conditions environnementales se créent, ceci n'explique pas encore
l'énorme expansion et la croissance renforcée des polypes des
coraux. Il existe de nombreux aquariums, qui d'une part peuvent
présenter de faibles quantités de substances nutritives, mais où les
coraux ne croissent pas obligatoirement plus vite ou ne vont pas
mieux dans l'ensemble.
Lorsque les bactéries se développent tellement qu'elles
forment déjà des dépôts mucosiques sur les vitres et la décoration,
il ne doit alors pas être étonnant que la quantité de phosphate
diminue nettement. Les biofilms ne peuvent pas épaissir à l'infini.
A partir d'un certain point, des parties se détachent et une
nouvelle couche pousse, jusqu'à ce que celle-ci soit à son tour
arrachée par le courant (Hûster 1996). Un écumage efficace
récupérera les restes de bactéries mortes et retirera ainsi
définitivement le phosphore du système. Sinon il se produirait de
nouveau une augmentation de la quantité de phosphates. Même si le
phosphate organique n'est plus transformé dans les bactéries en
phosphate inorganique – ce qui signifie, que nous ne pouvons pas le
mesurer – nous pourrions certainement conclure de la présence du
phosphore dans le bac par une croissance couronnée de succès des
algues et un nouvel assombrissement du tissu des coraux. Mais comme
décrit ce n'était pas le cas. C'est pour cette raison que le
récipient de collecte de l'écumeur constitue un composant important
de l'aquarium, sans lequel le retrait des phosphates ne
fonctionnerait certainement pas. Une quantité nettement plus
importante d'adsorbat dans le récipient de collecte de l'écumeur a
été constatée lors de l'utilisation de la méthode à base de vodka.
Sans doute ceci ne constitue qu'un revers de la médaille. Même si
par élimination des nitrates et des phosphates de meilleures
conditions environnementales se créent, ceci n'explique pas encore
l'énorme expansion et la croissance renforcée des polypes des
coraux. Il existe de nombreux aquariums, qui d'une part peuvent
présenter de faibles quantités de substances nutritives, mais où les
coraux ne croissent pas obligatoirement plus vite ou ne vont pas
mieux dans l'ensemble.  Suite à l'importante multiplication des bactéries par le
dosage d'éthanol, plus de bactéries sont extraites des biofilms et
se trouvent en liberté dans l'eau. Une partie de ces particules sont
rapidement écumées, mais une partie sert aussi de nourriture aux
coraux. La vigueur de l'expansion des polypes peut (mais ne doit
pas) indiquer une acquisition de nourriture. En règle générale
l'expansion des polypes comme chez les scléractiniaires durant la
phase nocturne est, lorsque la micro-faune et le zooplancton sortent
des pierres vivantes, nettement plus importante que durant le jour.
Suite à l'importante multiplication des bactéries par le
dosage d'éthanol, plus de bactéries sont extraites des biofilms et
se trouvent en liberté dans l'eau. Une partie de ces particules sont
rapidement écumées, mais une partie sert aussi de nourriture aux
coraux. La vigueur de l'expansion des polypes peut (mais ne doit
pas) indiquer une acquisition de nourriture. En règle générale
l'expansion des polypes comme chez les scléractiniaires durant la
phase nocturne est, lorsque la micro-faune et le zooplancton sortent
des pierres vivantes, nettement plus importante que durant le jour.
 Au plus tard à ce moment là, il faut commencer le
contrôle régulier de la quantité de nitrates et de phosphates.
Justement dans de très petits bacs avec un volume net de 100 à 200
litres la limite supérieure peut déjà être atteinte. Dans les
aquariums plus grands il est possible d'augmenter la quantité de
vodka d'1 ml chaque fois, à intervalle de trois jours. La chute de
la quantité de nitrates et de phosphates sert d'indicateur pour la
croissance des populations de bactéries. La quantité de phosphates
reflète surtout la croissance de toutes les bactéries hétérotrophes,
tandis que la décomposition des nitrates ne peut finalement
concerner qu'un rapport concernant les dénitrificateurs. Un bon test
phosphates ne doit pas manquer lors de l'utilisation de cette
méthode.
Au plus tard à ce moment là, il faut commencer le
contrôle régulier de la quantité de nitrates et de phosphates.
Justement dans de très petits bacs avec un volume net de 100 à 200
litres la limite supérieure peut déjà être atteinte. Dans les
aquariums plus grands il est possible d'augmenter la quantité de
vodka d'1 ml chaque fois, à intervalle de trois jours. La chute de
la quantité de nitrates et de phosphates sert d'indicateur pour la
croissance des populations de bactéries. La quantité de phosphates
reflète surtout la croissance de toutes les bactéries hétérotrophes,
tandis que la décomposition des nitrates ne peut finalement
concerner qu'un rapport concernant les dénitrificateurs. Un bon test
phosphates ne doit pas manquer lors de l'utilisation de cette
méthode. 
